已知室温下Mn(OH)2的溶解度为3.6×10-5mol·L-1,则室温下Mn(OH)2的溶度积Kspθ为()A、1.3×10-13B、2.6×10C、1.3×10-10D、2.6×10-10
题目
已知室温下Mn(OH)2的溶解度为3.6×10-5mol·L-1,则室温下Mn(OH)2的溶度积Kspθ为()
- A、1.3×10-13
- B、2.6×10
- C、1.3×10-10
- D、2.6×10-10
相似考题
更多“已知室温下Mn(OH)2的溶解度为3.6×10-5mol·L-1,则室温下Mn(OH)2的溶度积Kspθ为()A、1.3×10-13B、2.6×10C、1.3×10-10D、2.6×10-10”相关问题
-
第1题:
Al(OH)3的溶解度(S)与溶度积常数(Ksp)之间的关系是()A.S=(Ksp)1/2
B.(Ksp/4)1/2
C.(Ksp)1/3
D.(Ksp/27)1/4
参考答案:D
-
第2题:
Ca(OH)2和CaSO4的溶度积大致相等,则两物质在纯水中溶解度的关系是:A. SCa(OH)2 =SCaSO4
B.SCa(OH)2 <SCaSO4
C. SCa(OH)2 >SCaSO4
D.无法判断答案:C解析:解:Ca(OH)2属于AB2型,CaSO4属AB型的难溶电解质,两者类型不同,不能用溶度积直接比较。溶解度大小,必须通过溶解度与溶度积的关系式,计算出溶解度后才能进行比较。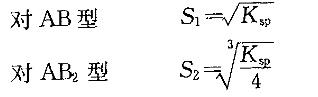 由此两式比较:S2>S1,即SCa(OH)2 >SCaSO4 。
由此两式比较:S2>S1,即SCa(OH)2 >SCaSO4 。
所以答案为C。 -
第3题:
25℃时AgCl在纯水中的溶解度为1.34×10-5mol/L,则该温度下AgCl的Ksp值为()。
- A、8.8×10-10
- B、5.6×10-10
- C、3.5×10-10
- D、1.8×10-10
正确答案:D -
第4题:
微溶化合物A2B3在溶液中解离平衡是:A2B3=2A+3B,今已测得B的浓度为3.0×10-3mol/L,则该微溶化合物的溶度积Ksp是()
- A、1.1×10-13
- B、2.4×10-13
- C、1.0×10-14
- D、2.6×10-11
正确答案:A -
第5题:
298K时,Mg(OH)2在水中溶解度(mol·L-1)[已知Mg(OH)2的Ksp为5.61×10-12]是()。
- A、1.77×10-4
- B、1.12×10-4
- C、2.36×10-6
- D、1.12×10-6
正确答案:B -
第6题:
25℃的CaCO3的溶解度为9.3×10-5mol/L-1,则CaCO3溶度积为()?
- A、8.6×10-9
- B、3.0×10-5
- C、1.9×10-10
- D、9.3×10-10
正确答案:A -
第7题:
已知KspΘ(Ag3PO4)=8.7×10-17,其在水中的溶解度s=()
- A、9.7×10-5mol·L-1
- B、4.2×10-5mol·L-1
- C、1.3×10-5mol·L-1
- D、7.3×10-5mol·L-1
正确答案:B -
第8题:
Mn(OH)2的KspΘ为1.9×10-13,在纯水中其溶解度为()mol·L-1;0.050molMn(OH)2(s)刚好在浓度为()mol·L-1,体积为0.5L的NH4Cl溶液中溶解。
正确答案:3.6×10-5;2.8 -
第9题:
Ag2SO4饱和水溶液中,溶解浓度为2.5×10-2mol·L-1,其溶度积Kspθ为(),Ag2SO4在0.5mol·L-1的AgNO3溶液中溶解度应为()mol.L-1。
正确答案: 6.25*10-5;5*10-3 -
第10题:
因为Ag2CrO4的溶度积(KSPθ=2.0×10-12)小于AgCl的溶度积(KSPθ=1.6×10-10),所以,Ag2CrO4必定比AgCl更难溶于水。
正确答案:错误 -
第11题:
单选题已知25℃的时Mn(OH)2的Ksp=4.0×10-14,则该温度下Mn(OH)2在水中的溶解度是()。A2.0×10-7mol·L-1
B2.0×10-6mol·L-1
C2.2×10-5mol·L-1
D2.2×10--4mol·L-1
正确答案: B解析: Mn(OH)2的溶解度为S(mol/L),Ksp=S×(2S)2=4.0×10-14,S=2.2×10-5mol·L-1 -
第12题:
填空题已知某Ba(OH)2溶液中,OH-的浓度为0.1mol·L-1,则Ba(OH)2的物质的量浓度为____.正确答案: 0.05mol·L-1解析:
氢氧化钡是强电解质,在溶液中能够全部溶解,且溶液中氢氧根离子的物质的量浓度为氢氧化钡物质的量浓度的两倍,因此氢氧化钡的物质的量浓度为0.05mol·L-1. -
第13题:
Ca(OH)2和CaSO4的溶度积大致相等,则两物质在纯水中溶解度的关系是:
A. SCa(OH)2 =SCaSO4
B.SCa(OH)2 <SCaSO4
C. SCa(OH)2 >SCaSO4
D.无法判断答案:C解析:解:Ca(OH)2属于AB2型,CaSO4属AB型的难溶电解质,两者类型不同,不能用溶度积直接比较。溶解度大小,必须通过溶解度与溶度积的关系式,计算出溶解度后才能进行比较。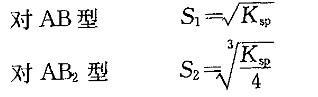 由此两式比较:S2>S1,即SCa(OH)2 >SCaSO4 。
由此两式比较:S2>S1,即SCa(OH)2 >SCaSO4 。
所以答案为C。 -
第14题:
AgCl的ksp=1.8×10-10,则同温下AgCl的溶解度为()。
- A、1.8×10-10mol/L
- B、1.34×10-5mol/L
- C、0.9×10-5mol/L
- D、1.9×10-3mol/L
正确答案:B -
第15题:
已知在25℃时氯化银的溶解度为1.34×10-5mol/L则氯化银的溶度积为()。
- A、1.34×10-5
- B、1.8×10-10
- C、3.6×10-10
- D、2.4×10-15
正确答案:B -
第16题:
对于难溶性强电解质Mg(OH)2,溶解度S与溶度积常数Ksp之间的关系为()
- A、Ksp=S2
- B、Ksp=2S2
- C、Ksp=3S2
- D、Ksp=4S2
正确答案:D -
第17题:
AgCl的Ksp=1.8×10-10则,AgCl溶解度的计算公式为S=Ksp1/2=(1.8×10-10)1/2。
正确答案:正确 -
第18题:
同温度下,将下列物质溶于水成饱和溶液,溶解度最大的是()
- A、AgCl(Ksp=1.8×10-18)
- B、Ag2Cr2O4(Ksp=1.1×10-12)
- C、Mg(OH)2(Ksp=1.8×10-10)
- D、Fe3(PO4)2(Ksp=1.3×10-22)
正确答案:C -
第19题:
当溶液的pH值为5时,下列哪种离子已完全沉淀:()(已知:K°sp(Al(OH)3)=5.0*10-33,K°sp(Cu(OH)2)=1.6*10-19,K°sp(Zn(OH)2)=4.5*10-17,K°sp(Mn(OH)2)=2.0*10-13,K°sp(Mg(OH)2)=8.9*10-12)
- A、Al3+
- B、Cu2+
- C、Mg2+
- D、Mn2+
- E、Zn2+
正确答案:A -
第20题:
已知25℃的时Mn(OH)2的Ksp=4.0×10-14,则该温度下Mn(OH)2在水中的溶解度是()。
- A、2.0×10-7mol·L-1
- B、2.0×10-6mol·L-1
- C、2.2×10-5mol·L-1
- D、2.2×10--4mol·L-1
正确答案:C -
第21题:
已知Sn(OH)2,Al(OH)3,Ce(OH)4的KspΘ分别为5.45×10-27,1.3×10-33,2.0×10-28,则它们饱和溶液的pH大小由小到大的顺序为()。
正确答案:Sn(OH)2Al(OH)3Ce(OH)4 -
第22题:
微溶化合物A2B3在溶液中的解离平衡是:A2B3==2A+3B。今已测得B的浓度为3.0×10-3mol/L,则该微溶化合物的溶度积Ksp是()
- A、1.1×10-13
- B、2.4×10-13
- C、1.0×10-14
- D、2.6×10-11
正确答案:A -
第23题:
单选题Kspθ(AgCl)=1.8×10-10,AgCl在0.010mol•L-1NaCl溶液中的溶解度为()。A1.8×10-10mol•L-1
B1.8×10-8mol•L-1
C1.3×10-5mol•L-1
D0.01mol•L-1
正确答案: A解析: 暂无解析
