给出下列基态原子或离子的价电子层电子组态,并用方框图表示轨道,填入轨道的电子则用箭头表示。
题目
给出下列基态原子或离子的价电子层电子组态,并用方框图表示轨道,填入轨道的电子则用箭头表示。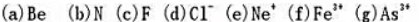
相似考题
参考答案和解析
答案: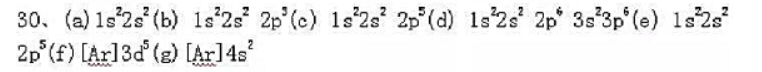
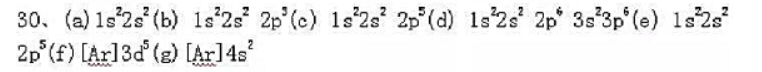
更多“给出下列基态原子或离子的价电子层电子组态,并用方框图表示轨道,填入轨道的电子则用箭头表示。 ”相关问题
-
第1题:
Fe元素基态有四个价电子分占不同的d轨道,但是Ca元素基态的两个价电子却占据同一轨道。下列说法错误的是
A.Fe的基态组态有四个电子分占不同的d轨道,是因为这种电子组态排斥能小
B.Ca的基态组态两个价电子占据同一轨道,是因为这种电子组态排斥能小
C.Fe的基态组态有四个电子分占不同的d轨道,符合Pauli原理和Hund规则
D.Ca的基态组态中其它未占据轨道能量很高,两个价电子占据同一轨道使得电子组态能量较低
Ca 的基态组态两个价电子占据同一轨道,是因为这种电子组态排斥能小 -
第2题:
写出原子序数为24的元素的名称,符号及其基态原子的电子排布式,价电子层排布式、单电子数。并用四个量子数分别表示每个价电子的运动状态.
答:第四周期, VIB ,铬 Cr : [Ar]3d 5 4s 1 四个量子数分别表示每个价电子的运动状态: 3, 2, 0, +1/2 ; 3, 2, +1, +1/2 ; 3, 2, -1, +1/2 ; 3, 2, +2, +1/2 ; 3, 2, -2, +1/2 ; 4, 0, 0, +1/2 ; -
第3题:
关于原子轨道的下列叙述正确的是
A.原子轨道不同于宏观物体的轨道。
B.某一原子轨道是电子的一种空间运动状态,即波函数
C.原子轨道表示电子在空间各点出现的概率
D.原子轨道表示电子在空间各点出现的概率密度
B -
第4题:
3 d 5 符号表示的意义是
A.3个 d 轨道上的 5 个电子
B.第三电子层上的 5 个d 轨道
C.第三电子层上一个d轨道有5个电子
D.第三电子层d轨道上的5个d电子
B -
第5题:
根据玻尔的理论,当处于基态的氢原子被能量为12.09 eV 的光子激发后,其电子的轨道半径为基态轨道半径的 倍。(说明:答案只能用整数表示,如:5)
1/16
