定压下,某反应A(S)+B(g)=2C(g)为放热反应,则该反应( )。A.△V>0,W>0 B.△V<0,W<0 C.△V>0,W<0 D.△V<0,W>0
题目
B.△V<0,W<0
C.△V>0,W<0
D.△V<0,W>0
相似考题
更多“定压下,某反应A(S)+B(g)=2C(g)为放热反应,则该反应( )。”相关问题
-
第1题:
某水力搅拌絮凝反应池,水力停留时间20min,水力损失0.35m,水温20℃。则改反应池的平均温度G值和GT值为(水温20℃时,水的黏度为1.002×10-3Pa·s,密度为998.2kg/m)( )。A、G=43.4s-1,GT=54067
B、G=43.4s-1,GT=64067
C、G=53.4s-1,GT=64067
D、G=53.4s-1,GT=54067答案:C解析: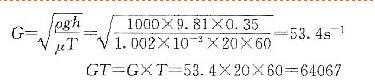
-
第2题:
ΔG<0的反应都是放热反应。
正确答案:错误 -
第3题:
已知反应C(s) + 2H2O(g) ←→ CO2(g) + 2H2(g) 的Kp为A,用A 表示下列各反应的平衡常数Kp 1/2C(s)+ H2O(g) ←→ 1/2CO2(g) + H2(g) Kp=()
正确答案:A1∕2 -
第4题:
反应H2(g)+Br2(g)⇋2HBr(g)在800K时平衡常数Kθ=3.8×105,1000K时平衡常数Kθ=1.8×103,则此反应()
- A、吸热反应
- B、放热反应
- C、无热效应的反应
- D、无法确定
正确答案:B -
第5题:
在298.15K和标准态时,下列反应均为非自发反应,其中在高温下仍为非自发反应的是()(不必计算)
- A、Ag2O(s) = 2Ag(s) + 1/2O2(g)
- B、N2O4(g) = 2NO2(g)
- C、Fe2O3(s) +3/2C(s) = 2Fe(s) +1/2CO2(g)
- D、6C(s) + 6H2O(g) = C6H12O6(s)
正确答案:D -
第6题:
在一定温度下,可逆反应C(s)+CO2(g)==2CO(g)的KΘ=2.0;当CO2(g)与CO(g)的分压皆为100kPa时,则该反应在同样温度时自发进行的方向为()。
正确答案:正向自发 -
第7题:
某反应A(g)+B(g)=C(g)的速率方程为v=k{c(A)}2c(B),若使反应密闭容积增大1倍,则其反应速率为原来的()。
- A、1/6
- B、8倍
- C、1/4
- D、1/8
正确答案:D -
第8题:
已知反应C(s)+O2(g)=CO2(g)的标准平衡常数为K1ө,CO(g)+1/2O2(g)=CO2((g)的标准平衡常数为Kө2,2C(s)+O2(g)=2CO(g)的标准平衡常数为Kө3,则Kө3与Kө1/和Kө2的关系为()
正确答案:(Kө1/Kө2)2 -
第9题:
在等压下化学反应A+B→C的△rHm>0,则该反应一定是()。
- A、吸热反应
- B、放热反应
- C、恒温反应
- D、无法确定吸热、放热或恒温反应
正确答案:D -
第10题:
如果某反应的△G<0,那么反应将会()
- A、是放热反应
- B、自动进行
- C、是吸热反应
- D、不发生
- E、处于平衡状态
正确答案:B -
第11题:
某化学反应恒温恒压下在可逆电池中完成时从环境吸热,则()
- A、ΔG>0
- B、ΔU>0
- C、ΔF>0
- D、ΔS>0
正确答案:D -
第12题:
单选题某反应A(g)+B(g)=C(g)的速率方程为v=K{c(A)}2c(B),若使反应密闭容积增大1倍,则其反应速率为原来的()。A1/6
B8倍
C1/4
D1/8
正确答案: A解析: 容积增大1倍,即浓度减小1倍。 -
第13题:
某水力搅拌絮凝反应池,水力停留时间20min,水力损失0.35m,水温20℃。则该反应池的平均温度G值和GT值为(水温20℃时,水的黏度为1.002×10-3Pa·S,密度为998.2kg/m)()。
- A、G=43.4s-1,GT=54067
- B、G=43.4s-1,GT=64067
- C、G=53.4s-1,GT=64067
- D、G=53.4s-1,GT=54067
正确答案:C -
第14题:
下列叙述正确的是()
- A、放热反应均为自发反应
- B、I2(g)的∆fGΘm(298.15)=0
- C、某反应的∆rGm>0,并不表示该反应在任何条件下都不能自发进行
- D、若反应的∆rHΘm和∆rGΘm均为正值,则升高温度∆rGΘm将增大
正确答案:C -
第15题:
在容器不变的密闭容器中,在一定条件下发生反应:2A(g)=B(g)+C(S),且达到化学平衡,当升高温度时其容器内气体的密度增大,则下列判断正确的是()
- A、若正反应是吸热反应,则A为非气态
- B、若正反应是放热反应,则A为气态
- C、若在平衡体系中加入少量C该平衡向逆反应方向移动
- D、压强对该平衡的移动无影响
正确答案:A,B -
第16题:
某化学反应A(g)+2B(s)→2C(g)的ΔrHm°<0,则下列判断正确的是:()
- A、仅在常温下,反应可以自发进行
- B、仅在高温下,反应可以自发进行
- C、任何温度下,反应均可以自发进行
- D、任何温度下,反应均难以自发进行
正确答案:B -
第17题:
反应H2(g)+I2(g)=2HI(g)的速率方程为ν= k C(H2)·C(I2),则该反应为基元反应。
正确答案:错误 -
第18题:
下列与化学反应能量变化相关的叙述正确的是()。
- A、生成物总能量一定低于反应物总能量
- B、放热反应的反应速率总是大于吸热反应的反应速率
- C、应用盖斯定律,可计算某些难以直接测量的反应焓变
- D、同温同压下,H2>(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同
正确答案:C -
第19题:
已知反应CO(g)+2H2(g)↔CH3OH(g)的KΘ(523K)=2.33×10-3,KΘ(548K)=5.42×10-4,则该反应是放热反应。当平衡后将系统容积压缩增大压力时,平衡向()反应方向移动;加入催化剂后平衡将()。
正确答案:正;不移动 -
第20题:
在等压下,进行一个反应 A + B→C,若∆rHm > 0,则该反应一定是()
- A、吸热反应
- B、放热反应
- C、温度升高
- D、无法确定
正确答案:D -
第21题:
反应2NaHCO3(s)=Na2CO3(s)+H2O(g)+CO2(g)在温度T时的标准平衡常数为90,该反应的压力平衡常数是()
- A、9119.25(kPa)
- B、924008(kPa)2
- C、9119.25
- D、924008
正确答案:B -
第22题:
已知下列反应的平衡常数:H(+ S (s) == H2S 2g)(g) K1;S (s) + O2 (g) == SO2 (g) K2;则反应H2(g)+ SO2 (g) == O2 (g) + H2S (g)的平衡常数为 ()。
正确答案:K=K1/K2 -
第23题:
单选题下列与化学反应能量变化相关的叙述正确的是()。A生成物总能量一定低于反应物总能量
B放热反应的反应速率总是大于吸热反应的反应速率
C应用盖斯定律,可计算某些难以直接测量的反应焓变
D同温同压下,H2>(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同
正确答案: C解析: 从能量变化的角度可将化学反应分为放热反应和吸热反应,放热反应产物的能量降低,吸热反应产物的能量升高;化学反应的速率由反应物的性质决定,也与某些外界条件有关,但与反应是否吸热、放热无关;盖斯定律是能量守恒原理的具体体现,因此只要确定反应物(温度、状态)和生成物(温度、状态),无论反应进行的途径如何,其总能量变化保持不变。
