对生物利用度实验研究的基本要求错误的是A、参比试剂应该有质量检验报告,并为在我国上市许可、有合法来源的药物制剂B、采用两制剂双周期交叉随机试验设计,间隔大于药物7~10个半衰期C、采样总点数不少于11个点,即服药前采空白血样1次,然后药时曲线峰前部分至少取4个点,峰后部分取6个或6个以上点D、采样时间持续3倍半衰期后或C的1/10以后E、对受试者没有年龄限制,多大年龄均可
题目
对生物利用度实验研究的基本要求错误的是
A、参比试剂应该有质量检验报告,并为在我国上市许可、有合法来源的药物制剂
B、采用两制剂双周期交叉随机试验设计,间隔大于药物7~10个半衰期
C、采样总点数不少于11个点,即服药前采空白血样1次,然后药时曲线峰前部分至少取4个点,峰后部分取6个或6个以上点
D、采样时间持续3倍半衰期后或C 的1/10以后
的1/10以后
E、对受试者没有年龄限制,多大年龄均可
相似考题
参考答案和解析
参考答案:E
更多“对生物利用度实验研究的基本要求错误的是A、参比试剂应该有质量检验报告,并为在我国上市许可、有合 ”相关问题
-
第1题:
制剂生物利用度研究时,关于参比制剂的说法错误的是A:参比制剂应具有安全性和有效性
B:进行相对生物利用度研究时,参比制剂为在研新制剂
C:进行绝对生物利用度研究时应选择上市的静脉注射剂作为参比制剂
D:进行相对生物利用度研究时应选择国内外同类上市主导产品作为参比制剂
E:参比制剂与受试制剂的剂量应相同答案:B解析:进行相对生物利用度研究时,应选择国内外同类上市主导产品为参比制剂,故B选项不正确。 -
第2题:
制剂生物利用度研究时,关于参比制剂的说法错误的是A.参比制剂应具有安全性和有效性
B.进行相对生物利用度研究时,参比制剂为在研新制剂
C.进行绝对生物利用度研究时应选择上市的静脉注射剂作为参比制剂
D.进行相对生物利用度研究时应选择国内外同类上市主导产品作为参比制剂
E.参比制剂与受试制剂的剂量应相同答案:B解析:进行相对生物利用度研究时,应选择国内外同类上市主导产品为参比制剂,故B项不正确。 -
第3题:
下列关于生物利用度和生物等效性试验的说法,正确的是( )。A.绝对生物利用度试验可以不用参比制剂作对照
B.生物利用度试验和生物等效性试验都必须用参比制剂作对照
C.生物利用度试验和生物等效性试验都可以不用参比试剂作对照
D.生物利用度试验可以不用参比制剂作对照,生物等效性试验则必须用参比制剂作对照
E.生物利用度试验必须用参比制剂作对照,生物等效性试验则可以不用参比制剂作对照答案:B解析: -
第4题:
对生物利用度实验研究的基本要求错误的是A.参比试剂应该有质量检验报告,并为在我国上市许可、有合法来源的药物制剂
B.采用两制剂双周期交叉随机试验设计,间隔大于药物7~10个半衰期
C.采样总点数不少于11个点,即服药前采空白血样1次,然后药时曲线峰前部分至少取4个点,峰后部分取6个或6个以上点
D.采样时间持续3倍半衰期后或C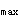 的1/10以后
的1/10以后
E.对受试者没有年龄限制,多大年龄均可答案:E解析: -
第5题:
对生物利用度实验研究的基本要求错误的是A.采样时间持续3个半衰期后或C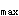 的1/10以后
的1/10以后
B.采样总点数不少于11个点,即服药前采空白血样1次,然后药时曲线峰前部分至少取4个点,峰后部分取6个或6个以上点
C.对受试者没有年龄限制,多大年龄均可
D.采用两制剂双周期交叉随机试验设计,间隔大于药物的7~10个半衰期
E.参比试剂应该有质量检验报告,并为在我国获得上市许可、有合法来源的药物制剂答案:C解析:
