一气缸内储有10 mol 的单原子分子理想气体,在压缩过程中,外力做功209 J,气体温度升高1 K,则气体内能的增量DE 为 J。
题目
一气缸内储有10 mol 的单原子分子理想气体,在压缩过程中,外力做功209 J,气体温度升高1 K,则气体内能的增量DE 为 J。
相似考题
更多“一气缸内储有10 mol 的单原子分子理想气体,在压缩过程中,外力做功209 J,气体温度升高1 K,则气体内能的增量DE 为 J。”相关问题
-
第1题:
一个气缸内有一定量的单原子分子理想气体,在压缩过程中外界做功209J,此过程中气体的内能增加120J,则外界传给气体的热量为( )J。A.-89
B.89
C.329
D.0答案:A解析:根据热力学第一定律Q=△E+W。注意到“在压缩过程中外界做功209J”,即系统对外做功W=-209J。又△E=120J,故Q=120+(-209)=-89J,即系统对外放热89J,也就是说外界传给气体的热量为-89J。 -
第2题:
有1mol刚性双原子分子理想气体,在等压过程中对外做功为W,则其温度变化ΔT为( )。A、 R/W
B、 W/R
C、 2R/W
D、 2W/R答案:B解析:质量一定的理想气体处于平衡态时的状态参量P、V、T之间的关系称为理想气体状态方程。理想气体状态方程式(克拉贝隆方程)为:pV=nRT,式中p是压力;V是体积;n是气体物质的量;T是热力学温度。pV=RT适用于1mol气体,该方程与气体的种类和工质经历的热力过程都无关。等压过程中,p=恒量,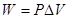
利用状态方程pV=RT,则有W=RΔT,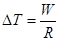
-
第3题:
一个气缸内有一定量的单原子分子理想气体,在压缩过程中对外界做功209J,此过程中气体的内能增加120J,则外界传给气体的热量为:
(A) -89J (B) 89J (C) 329J (13) 0答案:A解析:解:选A。根据热力学第一定律,dQ =dE+dA,由于dE=120J,dA=-209J,得到dQ=-89J,即系统对外放热89J,也就是说外界传给气体的热量为49J。
知识拓展:
1.热力学笫一定律
系统从外界吸收热量Q,一部分使系统的内能增ΔΕ;另 -部分系统对外做功.即 Q = (E2 -E1) +A
对于微小过程,
dQ =dE+dA
应用此定律时应注意以下几点:
①热力学第一定律不仅适用于气体,也适用于液体或固体,但我们只讨论理想气体。
②在系统状态变化过程中,各量的符号规定如下:
系统吸热,Q为正;系统放热Q为负。
系统对外做功A为正;外界对系统做功A为负。系统内能增加时,ΔΕ为正;减少时,ΔΕ为负。
③计算时式中各量需用统一单位制,在国际单位制中,三个量的单位都是J。 -
第4题:
—个气缸内有一定量的单原子分子理想气体,在压缩过程中对外界做功209J,此过程中气体的内能增加120J,则外界传给气体的热量为:A. -89J
B.89J
C. 329J
D. 0答案:A解析:热力学第一定律Q=E+W=(120—209)J=-89J。@niutk -
第5题:
1mol刚性双原子分子理想气体,当温度为T时,其内能为( )(式中R为摩尔气体常量,k为玻耳兹曼常量)。 答案:C解析:提示:1mol 刚性双原子分子理想气体内能
答案:C解析:提示:1mol 刚性双原子分子理想气体内能 。
。 -
第6题:
在一热力学过程中理想气体的内能增加了E2–E1=220J,其中从外界吸热Q=400J,则它对外做功A=()J。
正确答案:180 -
第7题:
已知1mol的某种理想气体(其分子可视为刚性分子),在等压过程中温度上升1K,内能增加了20.78J,则气体对外作功为();气体吸收热量为().(普适气体常量R=8.31.J/mol·K)
正确答案:8.31J;29.09J -
第8题:
1mol单原子理想气体,在300K时绝热压缩到500K,则其焓变ΔH约为()
正确答案:4157J -
第9题:
一定量的某种理想气体在等压过程中对外作功为200J。若此种气体为单原子分子气体,则该过程中需吸热()J;若为双原子分子气体,则需吸热()J。
正确答案:500;700 -
第10题:
已知1mol的某种理想气体(其分子可视为刚性分子),在等压过程中温度上升1K,内能增加了20.78J,则气体对外作功为(),气体吸收热量为()。(普适气体常量R=8.3lJ•mol-1•K-1)
正确答案:8.31J;29.09J -
第11题:
1mol单原子分子理想气体,从273K,202.65kPa,经pT=常数 的可逆途径压缩到405.3kPa的终态,该气体的ΔU为:()
- A、1702J
- B、-406.8J
- C、406.8J
- D、-1702J
正确答案:D -
第12题:
单选题1mol单原子理想气体,从温度300K绝热压缩到500K,则焓变为()。AΔH=0
BΔH=4157J
CΔH=2491J
DΔH=-2491J
正确答案: A解析: 暂无解析 -
第13题:
1mol刚性双原子分子理想气体,当温度为T时,其内能为: 答案:C解析:
答案:C解析:
-
第14题:
—个气缸内有一定量的单原子分子理想气体,在压缩过程中对外界做功209J,此过程中气体的内能增加120J,则外界传给气体的热量为:
A. -89J B.89J C. 329J D. 0答案:A解析:提示:根据热力学第一定律Q=ΔE+W,注意到“在压缩过程中外界做功209J”,即系统对外做功-209J。又ΔE=120J,故Q=120 + (-209) = --89J,即系统对外放热89J,也就是说外界传给气体的热量为-89J。 -
第15题:
对于一定量的理想气体在某一过程中,从外界吸收热量2.5X104 J,气体对外做功1.0×104J,则该理想气体( )。
A.温度降低,密度增大
B.温度降低,密度减小
C.温度升高,密度增大
D.温度升高.密度减小答案:D解析:由AE=W+Q=一1.0x104 J+2.5x104 J=1.5x104 J,可知气体内能增加,温度升高。由于气体对外做功,所以体积增大,密度减小。 -
第16题:
刚性密封容器中放有1 mol单原子理想气体,在25℃下,当系统经历某过程后△S=10
J·K-1,则系统的△U相应变化了()J。A.1.0
B.25
C.298.15
D.1000答案:D解析: -
第17题:
一个气缸内储存有一定量的单原子分子理想气体,在压缩过程中外界做功209J, 此过程气体内能增量120J,外界传给气体的热量为( )J。
A. -89 B. 89 C. 329 D. 0答案:A解析:提示:热力学第一定律Q=ΔE+W = (120-209)J = -89J。 -
第18题:
1mol的单原子分子理想气体,在1atm的恒定压强下,从0℃加热到100℃,则气体的内能改变了()J.(普适气体常量R=8.31J·mol-1·k-1)
正确答案:1.25×103J -
第19题:
1mol单原子理想气体,从温度300K绝热压缩到500K,则焓变为()。
- A、ΔH=0
- B、ΔH=4157J
- C、ΔH=2491J
- D、ΔH=-2491J
正确答案:B -
第20题:
已知lmol的某种理想气体(其分子可视为刚性分子),在等压过程中温度上升1K,内能增加了20.78J,则气体对外作功为()气体吸收热量为()。(普适气体常量R=8.31.J•mol-1•K-1)
正确答案:8.31J;29.09J -
第21题:
一定量H2气(视为刚性分子的理想气体),若温度每升高1K,其内能增加41.6J,则该H2气的质量为()。(普适气体常量R=8.31J•mol-1•k-1)
正确答案:4.0×10-3kg -
第22题:
lmol的单原子分子理想气体,在1atm的恒定压强下,从0℃加热到100℃,则气体的内能改变了()J。(普适气体常量R=8.31J•mol-1•k-1)
正确答案:1.25×103 -
第23题:
1mol理想气体经绝热自由膨胀使体积增大10倍,则体系的熵变为()
- A、ΔS=0J.K-1
- B、ΔS=19.1J.K-1
- C、ΔS〉19.1J.K-1
- D、ΔS=8.314J.K-1
正确答案:B -
第24题:
单选题一个气缸内有一定量的单原子分子理想气体,在压缩过程中对外界做功209J,此过程中气体的内能增加120J,则外界传给气体的热量为:()A-89J
B89J
C329J
D0
正确答案: D解析: 暂无解析
