往50 mL稀硫酸和稀盐酸的混合溶液中加入2.137 5 g氢氧化钡粉末,充分反应后进行过滤,滤液的pH=13,其沉淀干燥后质量为
题目
相似考题
更多“往50 mL稀硫酸和稀盐酸的混合溶液中加入2.137 5 g氢氧化钡粉末,充分反应后进行过滤,滤液的pH=13,其沉淀干燥后质量为”相关问题
-
第1题:
有一杯50ml 的溶液,浓度是60mg/ml,现向杯中加入50ml 的水,充分混合后, 倒出50ml 溶液,重复上述操作3 次后, 杯中溶液浓度变成( )mg/ml。
A 7.5 B 15 C 20 D 30
正确答案:A
-
第2题:
向某溶液中加入过量盐酸生成白色沉淀,过滤后向滤液中加入过量的氨水(使溶液呈碱性).又有白色沉淀生成:再过滤后向滤液中加入碳酸钠溶液,又生成白色沉淀。则原溶液中含有的离子可能是()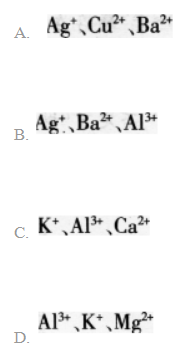 答案:B解析:
答案:B解析:
-
第3题:
含有碳酸镁、石英两种杂质的石灰石1g,加入浓度为36%的盐酸5g,充分反应后过滤,得到0.29g沉淀和5.38g滤液。该石灰石中CaCO3的质量分数()(原子量Ca:40,Mg:24,C://12,O:16,Cl:35.5,H:1,Si:28)
- A、29%
- B、36%
- C、50%
- D、52%
正确答案:C -
第4题:
下列各组中两物质的溶液混合恰好完全反应并生成沉淀,将沉淀滤去后的溶液蒸发,可得到食盐晶体的是()
- A、硫酸钠和氢氧化钡
- B、氢氧化钡和氯化钾
- C、硝酸银和氯化钡
- D、氯化钡和硫酸钠
正确答案:D -
第5题:
向一含的四种离子(主要离子)的混合溶液中滴加AgNO3溶液,至不再有沉淀析出为止.过滤,当用稀硝酸处理沉淀时,砖红色沉淀溶解得橙色溶液,但仍有白色沉淀.滤液呈紫色,用硫酸酸化后,加入Na2SO3,则紫色逐渐消失.作"焰色反应"透过蓝色钴玻璃可以看到紫色火焰.指出上述溶液有何物质?并写有关反应方程式
正确答案: 混合液中含有:KClK2CrO4KMnO4
当加入AgNO3:Ag++Cl-=AgCl↓(白)
2Ag++CrO42-=Ag2CrO4↓(砖红)
加入稀HNO3:AgCl不溶
2Ag2CrO4+2H+=4Ag++Cr2O72-(橙红)+H2O
加入H2SO4酸化,再加入Na2SO3,
2MnO4-+5SO32-+6H+=2Mn2++5SO42-+3H2O -
第6题:
阿司匹林与氢氧化钠试液共热,主要发生()反应放冷后,加入稀硫酸试液立即析出白色沉淀,此白色沉淀是()将溶液滤过,滤液中加入乙醇和浓硫酸,并加热,即产生有特殊香味的()。
正确答案:水解;水杨酸;醋酸乙酯 -
第7题:
取延胡索粉末1g,加N/2硫酸液10ml,振摇片刻,滤过。取滤液2ml,加1%高铁氰化钾溶液0.4ml与1%三氯化铁溶液0.3ml的混合液,即显()色,渐变()色,放置后底部有较多()色沉淀。
正确答案:深绿;深蓝;深蓝 -
第8题:
填空题往物质的量浓度相同的氯化铜、三氯化铁和氯化铝的混合溶液中,加入过量铁粉,充分反应后进行过滤,滤纸上得到的反应产物是____,滤液中浓度最大的金属离子是____.正确答案: Cu,Fe2+解析:
铁粉还原Cu2+生成Cu,铁粉还原Fe3+生成Fe2+,同时铁粉在反应中也变为Fe2+,因此滤液中浓度最大的金属离子是Fe2+. -
第9题:
单选题99mL0.1mol/L盐酸和101mL0.05mol/L氢氧化钡溶液相混合后,溶液的pH值为()A1.7
B10.7
C11
D11.3
正确答案: D解析: 暂无解析 -
第10题:
填空题取某钻井液样品50mL,做氯离子含量的测定,钻井液样品经滤纸过滤后获得5mL滤液,取2mL滤液做滴定,耗去0.05mol/L的AgNO溶液20mL,则钻井液样品中氯离子的质量浓度为()。正确答案: 17.75×10mg/L解析: 暂无解析 -
第11题:
填空题有一包固体粉末,由下列物质中若干种均匀混合而成:Ba(NO3)2、CaCO3、Na2S、CuSO4、BaCl2,有关实验过程及记录如下:(1)将粉末溶于水,得到蓝色溶液和白色沉淀.过滤后将沉淀洗涤、烘干,称重质量为m克;(2)向滤出的沉淀中加入盐酸,沉淀不溶解;(3)把滤液分成三等份,第一份加稀HNO3和AgNO3溶液,无白色沉淀生成;第二份加入稀H2SO4,无明显现象:第三份加入过量Ba(NO3)2溶液,有白色沉淀生成,把沉淀滤出后洗涤,烘干,称重质量为m克.试判断此白色粉末由____混合而成,它们的物质的量之比为____.正确答案: Ba(NO3)2和CuSO4,1:4解析:
含Cu2+的溶液颜色为蓝色,粉末溶于水后得到蓝色溶液,则粉末中有CuSO4;既然含有CuSO4,则必然不含Na2S,否则两者之间会反应生成黑褐色沉淀CuS,由(2)知,粉末中不含有CaCO3;滤液加稀HNO3和AgNO3溶液,无白色沉淀生成,则溶液中不含有BaCl2;滤液加入稀H2SO4,无明显现象,说明沉淀过滤后,溶液中已经不含有Ba2+;由于粉末溶于水后得白色沉淀,则粉末中含有Ba(NO3)2.滤液加入过量的Ba(NO3)2溶液有白色沉淀生成,说明溶液中仍然含有SO42-,CuSO4是过量的,反应方程式为Ba(NO3)2+CuSO4=BaSO4↓+Cu(NO3)2,刚开始溶于水时产生白色沉淀BaSO4为m克,则各自消耗Ba(NO3)2和CuSO4一份,过滤后剩余的滤液分成三等份,其中一份加入过量Ba(NO3)2溶液,仍然有白色沉淀为m克,则滤液中含CuSO4三份,故Ba(NO3)2和CuSO4的物质的量之比为1:4. -
第12题:
问答题有KCl和KBr的混合物3.87克,溶于水配成溶液,向溶液中加入足量的AgNO3溶液,产生沉淀,经过滤干燥得6.63克沉淀,则混合物中钾元素的质量分数是多少?(AgBr不溶于水)正确答案: 因为 K———Ag Δm
39 109 69克
X (6.63—3.87)克
X=1.56克
钾元素的质量分数为:1.56克/3.87克=40.3%解析: 暂无解析 -
第13题:
等体积混合0.1 mol/L盐酸和0.06 mol/L氢氧化钡溶液,混合后溶液的pH=____________.答案:解析:12【解题指要】
(1)设酸和碱溶液的体积均为1 L,则盐酸溶液中含HCl为0.1 mol/L×1 L=0.1 mol;
Ba(OH)2溶液中含Ba(OH)2为0.06 mol/L×l L=0.06 mol.
(2)两溶液混合时,要发生化学反应
因此,混合后可能有以下三种情况:
①恰好完全反应.因BaCl2是强酸强碱盐,所以溶液显中性.
②酸有剩余,溶液显酸性.
③碱有剩余,溶液显碱性.
究竟属于哪一种情况,需经计算才能知道.
设与盐酸完全反应需Ba(OH)2xmol,则
所以Ba(OH)2剩余:0.06 mol-0.05 mol=0.01mol.
(3)计算混合后溶液的pH.

OH一的物质的量浓度为0.005 mol/L×2=0.01mol/L,则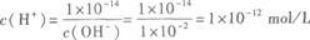
即pH=12. -
第14题:
能用离子方程式H++OH-H2O表示的反应是( )。A.稀盐酸和氢氧化钠反应
B.稀氨水与稀盐酸
C.稀硫酸和氢氧化钾溶液反应
D.稀硫酸和氢氧化钡溶液反应答案:A,C解析: -
第15题:
取某钻井液样品50mL,做氯离子含量的测定,钻井液样品经滤纸过滤后获得5mL滤液,取2mL滤液做滴定,耗去0.05mol/L的AgNO溶液20mL,则钻井液样品中氯离子的质量浓度为()。
正确答案:17.75×10mg/L -
第16题:
含有ⅠA和ⅠB两种离子的混合液,向其中加入氯化钠溶液产生白色沉淀A,过滤分离后,向A中加入氨水部分溶解为无色溶液B,往其中加硝酸产生白色沉淀C,而部分沉淀A加氨水后转化为灰黑色沉淀D.将D溶于硝酸形成无色溶液,往此溶液中加入KI产生桔红色沉淀E.A,B,C,D,E各为何物。
正确答案:A.AgCl和Hg2cl2
B.Ag(NH3)2+
C.AgCl
D.HgNH2Cl和Hg
E.HgI2 -
第17题:
有KCl和KBr的混合物3.87克,溶于水配成溶液,向溶液中加入足量的AgNO3溶液,产生沉淀,经过滤干燥得6.63克沉淀,则混合物中钾元素的质量分数是多少?(AgBr不溶于水)
正确答案: 因为 K———Ag Δm
39 109 69克
X (6.63—3.87)克
X=1.56克
钾元素的质量分数为:1.56克/3.87克=40.3% -
第18题:
在盛有无色溶液A的试管中,加数滴NaCl溶液,产生白色沉淀,再加入几滴氨水,摇动后沉淀消失,再加入几滴KBr溶液后,又有谈黄色沉淀产生,再加入Na2S2O3溶液后,沉淀又消失,推断A为(),其有关离子反应式(),(),(),()。
正确答案:AgNO3;Ag++Cl-=AgCl;AgCl+2NH3=[Ag(NH3)2]++Cl-;[Ag(NH3)2]++Br-=AgBr2+NH3;AgBr+2S2O32-=[Ag(S2O3)2]3-+Br- -
第19题:
纸绝缘聚合度检测结果必须满足下列哪些条件才能认为结果符合要求()。
- A、两个DPv相差不应超过其平均值的2.5%
- B、两个DPv相差不应超过其平均值的2%
- C、粘度测量后,用3号耐酸过滤漏斗过滤溶液。用稀盐酸洗涤过滤器和沉淀物,然后用蒸馏水洗,经过110℃左右烘箱干燥后,在干燥器中冷却并称量,不溶残渣应当少于试样原始重量的5%
- D、粘度测量后,用3号耐酸过滤漏斗过滤溶液。用稀盐酸洗涤过滤器和沉淀物,然后用蒸馏水洗,经过110℃左右烘箱干燥后,在干燥器中冷却并称量,不溶残渣应当少于试样原始重量的10%
正确答案:A,C -
第20题:
单选题下列过程中,不发生颜色变化的是( ).A将无水硫酸铜加入水中
B将一氧化氮和氧气混合
C往稀硫酸溶液中加入过量铁屑
D往稀硫酸溶液中通入少量氨气
正确答案: C解析:
A项,无水硫酸铜加入水中使溶液变蓝;B项,NO和O2混合生成红棕色NO2气体;C项,铁屑溶于稀硫酸后产生浅绿色的Fe2+;D项,氨气通入无色的稀硫酸无颜色变化,因为(NH4)2SO4在溶液中无色. -
第21题:
填空题将pH=1的盐酸溶液1.0mL与pH=13的NaOH溶液1.0mL混合后,假定混合后的体积是两种溶液的体积之和,则该混合溶液的pH约为____.正确答案: pH=7解析:
根据已如条件计算可知,混合前两溶液中H+和OH-物质的量的浓度相等,刚好中和完全,因此混合后溶液的pH=7,呈中性. -
第22题:
填空题将54.4g铁和氧化铁的混合粉末投入到适量的稀硫酸中,充分反应后收集到4.48L(标准状况下)氢气并测得溶液中既没有Fe3+也没有固体物质残留,则原混合粉末中铁和氧化铁的质量分别是____g和____g,反应中硫酸消耗掉____mol,反应后得到硫酸亚铁的物质的量是____mol.正确答案: 22.4,32,0.8,0.8解析:
由分析题意可知,最终剩余的铁和三价铁离子恰好完全反应.混合物中的铁的计算分为两部分,一部分是与稀硫酸反应生成氢气,另一部分是和三价铁离子(剩余部分的稀硫酸氧化铁全部转化为三价铁离子)完全反应,生成二价铁离子. -
第23题:
填空题阿司匹林与氢氧化钠试液共热,主要发生()反应放冷后,加入稀硫酸试液立即析出白色沉淀,此白色沉淀是()将溶液滤过,滤液中加入乙醇和浓硫酸,并加热,即产生有特殊香味的()。正确答案: 水解,水杨酸,醋酸乙酯解析: 暂无解析
